CDE文章解讀:預(yù)防用 mRNA 疫苗脂質(zhì)納米顆粒質(zhì)量研究
核酸藥物歷經(jīng)幾十年的發(fā)展,始終受限于遞送系統(tǒng)這一關(guān)鍵技術(shù)瓶頸。脂質(zhì)納米顆粒(lipid nanoparticle, LNP)技術(shù)的研發(fā)極大地推動了核酸藥物的發(fā)展。新冠疫情期間 mRNA 疫苗的大放異彩更是將核酸藥物的研發(fā)和產(chǎn)業(yè)化推向了前所未有的高度。盡管 mRNA-LNP 的制備工藝步驟簡單、周期較短,但短短幾分鐘內(nèi)就可能存在復(fù)雜的相變。近年來,國內(nèi)外監(jiān)管機構(gòu)相繼發(fā)布了 mRNA 疫苗的技術(shù)指南,如國家藥品監(jiān)督管理局藥品審評中心于 2020 年 8 月發(fā)布《新型冠狀病毒預(yù)防用 mRNA 疫苗藥學(xué)研究技術(shù)指導(dǎo)原則(試行)》,世界衛(wèi)生組織(World Health Organization, WHO)2021 年 12 月發(fā)布的“Evaluation of the quality, safety and efficacy of messenger RNA vaccines for the prevention of infectious diseases: regulatory considerations”,美國藥典(USP)于 2022 年 2 月發(fā)布了題為“mRNA 疫苗質(zhì)量分析方法”的指南草案等,初步建立了 mRNA 疫苗的質(zhì)量評價標(biāo)準。
1999 年 3 月,國際人用藥品注冊技術(shù)要求協(xié)會(The International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use, ICH)為了協(xié)調(diào)歐盟、美國、日本等主要市場的監(jiān)管標(biāo)準,減少研發(fā)和審批壁壘,制定了《質(zhì)量標(biāo)準:生物技術(shù)產(chǎn)品及生物制品的檢測方法和驗收標(biāo)準》,作為生物技術(shù)藥物的指導(dǎo)原則,簡稱 ICH Q6B。ICH Q6B 對于生物制品強調(diào)了生產(chǎn)工藝全過程控制,同時認為,在質(zhì)量標(biāo)準中納入哪些質(zhì)控項目需要根據(jù)產(chǎn)品工藝特點、特性特點及其與安全有效性、質(zhì)量可控性的相關(guān)性予以確定。國家藥品監(jiān)督管理局藥品審評中心研究團隊根據(jù) ICH Q6B 理念,發(fā)表了《預(yù)防用 mRNA 疫苗脂質(zhì)納米顆粒質(zhì)量研究及質(zhì)量控制藥學(xué)評價的考慮》,從藥學(xué)評價角度對上述結(jié)構(gòu)特點、變化趨勢等進行初步探討,對結(jié)構(gòu)特征需要額外開展的研究工作提出建議,希望為預(yù)防用 mRNA 疫苗研發(fā)、生產(chǎn)及產(chǎn)品質(zhì)量提升提供借鑒。

研究建議
一、粒徑分布和顆粒濃度
粒徑大小是決定納米藥物的半衰期和在體內(nèi)分布的關(guān)鍵參數(shù),粒徑較小的納米藥物更可能會逃脫吞噬細胞的攝取。藥用脂質(zhì)體的顆粒尺寸一般不大于 100 nm,尤其是在腸胃外給藥的情況下。此外,顆粒濃度作為納米藥物分析中另一個非常重要的參數(shù),直接影響產(chǎn)品的給藥劑量和治療效果。
本文研究建議:采用多種檢測方法對關(guān)鍵指標(biāo)進行研究,例如:粒徑檢測,除常規(guī)的 DLS 法,建議采用 NTA、電鏡計數(shù)、凝膠色譜、納米流式等方法以及總粒子計數(shù)等方法。
NanoFCM 可在單顆粒水平實現(xiàn)納米藥物的粒徑分布和顆粒濃度的無標(biāo)記分析,通過靈活的圈門策略能夠定向圈出特定粒徑范圍內(nèi)顆粒的分布和占比情況。如圖 1 所示,LNPs 樣本的粒徑分布為 40-150 nm,平均值 84.1 nm;通過單顆粒計數(shù)方法標(biāo)定該樣本中顆粒濃度為 2.67E+12 particles/mL。
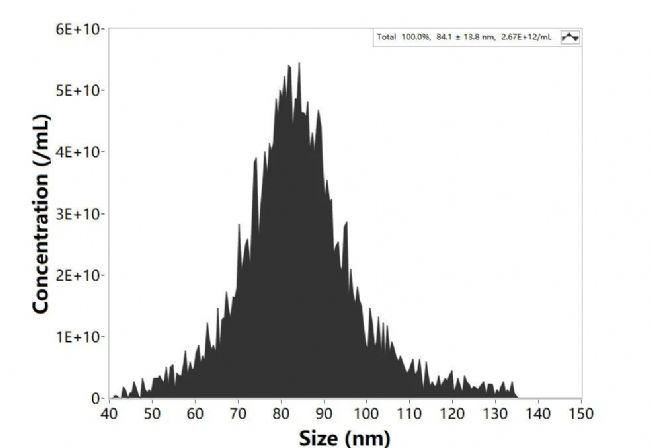
圖1. mRNA LNPs 的粒徑和濃度分析
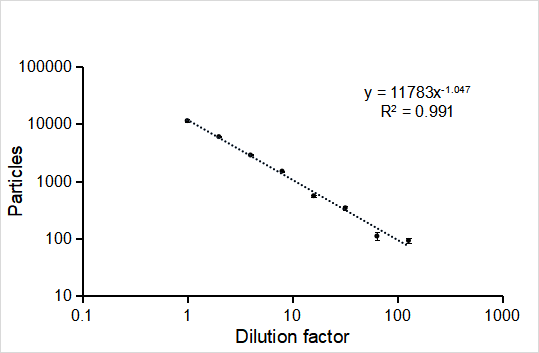
圖2. mRNA LNPs 的濃度梯度稀釋曲線
二、mRNA 空載體數(shù)
在 mRNA-LNP 的制備過程中,部分脂質(zhì)可能未能成功包封 mRNA,形成空載體。這些空載體的存在會影響 mRNA 的封裝率和遞送效率。
本文研究建議:開展制劑過程中不同階段(如包封、pH 調(diào)整及超濾等過程中)產(chǎn)物不含 mRNA 的空載體數(shù)、顆粒數(shù)及顆粒濃度、脂質(zhì)成分均勻性等研究。
NanoFCM 可以通過熒光標(biāo)記等手段,區(qū)分包封了 mRNA 的顆粒和空載體。mRNA LNPs 顆粒通過探測區(qū)時,同時產(chǎn)生側(cè)向散射 SS 和熒光 FL 信號,有 SS 信號無對應(yīng)的 FL 信號的顆粒為空的 LNP,在二維散點圖中,mRNA LNPs 和空載 LNPs 清晰地分成兩個群體(圖3)。基于納米流式檢測技術(shù)僅需 1 min 即可實現(xiàn) mRNA-LNPs 樣本中空載率的準確定量,且經(jīng)過梯度稀釋驗證線性良好,證明結(jié)果的準確性(圖4)。此外,mRNA LNPs 空載率檢測已被納入石藥集團的創(chuàng)新技術(shù)。(詳見往期文章:《重磅|石藥集團發(fā)布 mRNA-LNPs 的創(chuàng)新制備方法》)
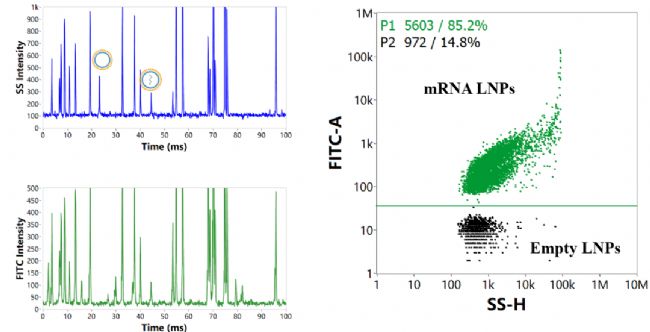
圖3. NanoFCM 對 mRNA-LNPs 的空載率表征
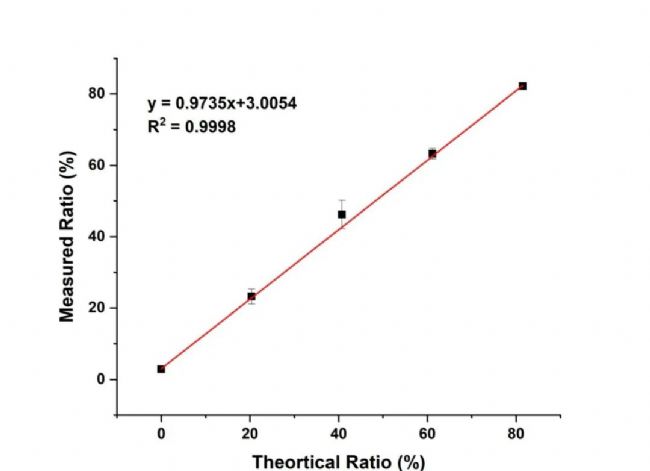
圖4. mRNA LNPs 的裝載率實測與理論線性關(guān)系
三、mRNA 在 LNP 分布位置
本文研究建議:可開展制劑過程中不同階段(如包封、pH 調(diào)整及超濾等過程中)產(chǎn)物 mRNA 在 LNP 中分布位置的拓展性、探索性研究。
通常大家認為 mRNA 要么被包封在 LNP 里面,要么游離在溶液中,有沒有第三種形態(tài)存在呢?NanoFCM憑借卓越的單分子熒光檢測技術(shù)給出了顛覆性答案——mRNA 竟會“黏”在 LNP 表面!通過創(chuàng)新的核酸染料標(biāo)記策略,首次揭示了 mRNA-LNP 體系的五種存在形態(tài):游離 mRNA、空殼 LNP、包封 LNP 以及表面吸附 mRNA 的 LNP。NanoFCM 基于跨膜及非跨膜核酸染料對 mRNA 疫苗進行標(biāo)記,并結(jié)合 RNase 處理策略以實現(xiàn)疫苗樣本中 mRNA 分子的精準定位分析。圖5詳細概括了通過不同的標(biāo)記策略來進行核酸定位分析,相關(guān)人員可以采用同樣的標(biāo)記策略對 mRNA LNPs 進行核酸定位分析,進而優(yōu)化制劑配方和下游工藝流程,盡可能最大化地實現(xiàn) mRNA 的有效裝載,獲得高純度、高裝載效率的 mRNA LNPs 產(chǎn)品。

圖5. 核酸定位分析
四、包封率檢測
本文研究建議:包封率檢測,除常規(guī)使用的 RiboGreen 法,建議采用不同或互補的檢測方法,如超速離心、超濾、凝膠色譜等進一步確證,在確證研究中采用不同條件包括極端條件處理后的產(chǎn)品以驗證相關(guān)檢測方法的適用性和產(chǎn)品的降解途徑等。
NanoFCM 在單次上樣中同時獲得游離 mRNA 與 LNP 包封 mRNA 的熒光信號。基于熒光強度與核酸分子的拷貝數(shù)成線性正相關(guān)關(guān)系,直接定量分析每個納米顆粒內(nèi) mRNA 拷貝數(shù)。根據(jù)藥典中關(guān)于包封率的定義,NanoFCM 可以快速計算包封率。NanoFCM 專業(yè)版的軟件能夠一鍵生成核酸拷貝數(shù)和包封率的結(jié)果,以極致的時間與樣本利用率,重新定義納米樣品檢測的生產(chǎn)力標(biāo)準(圖6)。
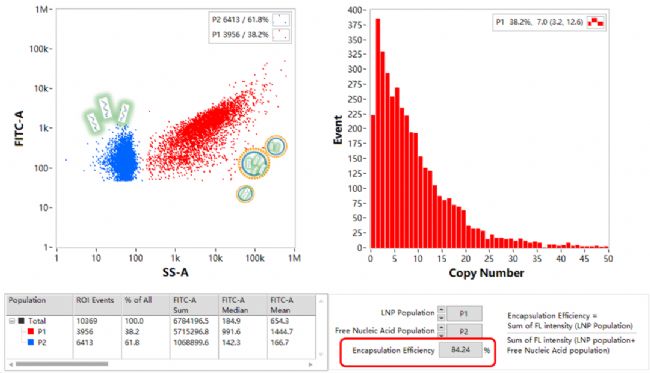
圖6. NanoFCM 對 mRNA-LNPs 的核酸拷貝數(shù)和包封率表征
展望
本文對 mRNA-LNP 質(zhì)量研究的建議為疫苗的研發(fā)和生產(chǎn)提供了明確的方向。NanoFCM 憑借其獨特的優(yōu)勢,可在單顆粒水平實現(xiàn)核酸藥物粒徑分布、顆粒濃度、空殼率、藥物包封率及核酸定位等參數(shù)的定量分析。通過 NanoFCM 的應(yīng)用,研究人員可以更全面地了解 mRNA-LNP 的質(zhì)量屬性,優(yōu)化生產(chǎn)工藝,提高疫苗的安全性和有效性,為 mRNA 疫苗的研發(fā)和臨床應(yīng)用提供有力保障。
- ApogeeFlow納米流式儀助力微生物檢測技術(shù)革新
- CDE文章解讀:預(yù)防用 mRNA 疫苗脂質(zhì)納米顆粒質(zhì)量研究
- ApogeeFlow納米流式攜手梅奧診所推動細胞外囊泡(EV)分析新突破
- 文獻解讀:細胞外囊泡和脂質(zhì)納米顆粒的條形碼雜交助力藥物靶向遞送
- 納米流式檢測技術(shù) (nFCM) 評估六種膜燃料標(biāo)記細胞外囊泡的性能研究
- 模擬HIV膜融合機制開發(fā)的創(chuàng)新病毒樣顆粒T-FVLPmCAR載體技術(shù)及應(yīng)用
- 納米流式技術(shù)在單顆粒水平定量分析sEVs表面的唾液酸中的應(yīng)用
- ApogeeFlow納米流式協(xié)助Mayo Clinic揭示早期結(jié)直腸癌新生物標(biāo)志物