小鼠模型在揭示二硫鍵調控抗病毒免疫機制中的應用
固有免疫系統是機體抵御病原體入侵的第一道防線,在抗病毒免疫中發揮著重要作用。RNA病毒因其高變異性,常常引發致命的大流行病,對人類健康構成重大威脅。固有免疫系統通過識別病原體的特異性分子模式,迅速啟動免疫反應,從而阻止病毒的進一步擴散。RIG-I(Retinoic Acid-Inducible Gene I)作為一種重要的胞質RNA感受器,在識別病毒雙鏈RNA(dsRNA)后,能夠觸發抗病毒免疫應答。然而,RIG-I的激活機制及其動態調控過程仍存在許多未解之謎。近日,由浙江大學張龍教授領導的研究團隊發現,RIG-I分子間C864-C869二硫鍵的形成對于其相分離及其介導的抗病毒免疫應答至關重要。此外,研究還開發了靶向穩定或抑制RIG-I二硫鍵形成的干預策略,為抗病毒治療及自身免疫性疾病的治療提供了新的思路。這項研究成果于2025年4月發表在國際知名期刊《Nature Cell Biology》。

研究材料與方法
為了深入探究C864-C869分子間二硫鍵的形成在RIG-I介導的固有免疫應答中的作用,本研究使用RIG-I分子間二硫鍵形成缺陷型基因敲入小鼠模型(Rig-IC865S/C865S)進行了小鼠水平的驗證。該敲入小鼠模型由賽業生物公司通過CRISPR-Cas9 技術構建。為了生成敲入后代,將針對小鼠Rig-I基因的gRNA、含有p.C865S(TGC至AGC)突變和一個同義突變p.S871=(AGC至TCT)的供體寡核苷酸以及Cas9 共同注射到受精卵中。
技術路線
質譜分析發現病毒刺激引起RIG-I分子間C864-C869二硫鍵的形成
↓
通過基因編輯技術構建Knock-in小鼠,驗證C864-C869二硫鍵的功能
↓
使用遺傳密碼拓展技術,在RIG-I C864位點引入非天然氨基酸,實現分子間二硫鍵的穩定交聯
↓
開發靶向抑制RIG-I二硫鍵形成的干擾肽
研究結果
(1) RIG-I二硫鍵的鑒定與驗證
研究團隊發現病毒刺激能夠誘導RIG-I分子間二硫鍵的形成。為了確定RIG-I分子間二硫鍵形成的位點,研究人員對有無SeV病毒刺激情況下的RIG-I進行了質譜分析。質譜結果顯示,在SeV病毒刺激下,RIG-I蛋白分子間能夠形成C864-C869 位點的二硫鍵;而在沒有病毒刺激時,未檢測到分子間二硫鍵的形成。
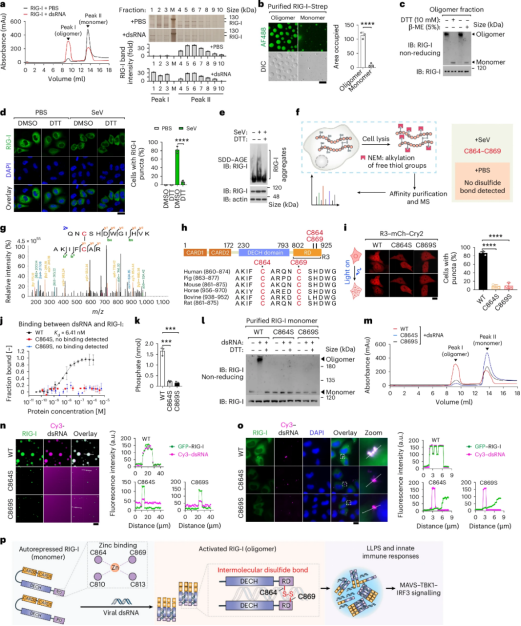
圖1. RNA病毒刺激誘導RIG-I蛋白間形成C864-C869位點的分子間二硫鍵
(2)C864-C869分子間二硫鍵的形成對于RIG-I介導的固有免疫應答至關重要
研究團隊使用賽業生物公司提供的RIG-I分子間二硫鍵形成缺陷型基因敲入小鼠模型進行了小鼠水平的驗證。探究結果發現:C865S點突變(對應人C864S突變)導致RIG-I寡聚化和凝聚體形成缺陷,顯著抑制固有免疫反應,使小鼠對VSV病毒感染的易感性增加并伴隨死亡率上升。
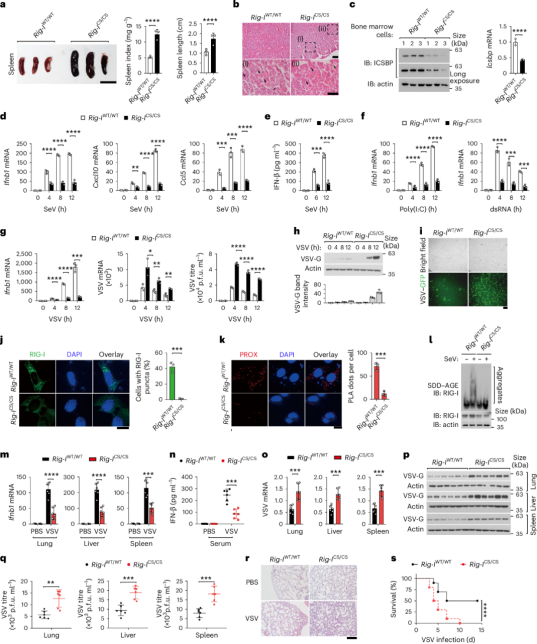
圖2. C864-C869分子間二硫鍵的形成對于RIG-I介導的固有免疫應答至關重要
(3)靶向RIG-I C864-C869分子間二硫鍵以調控宿主抗病毒免疫應答
研究人員開發了靶向穩定或抑制RIG-I C864-C869二硫鍵形成的干預策略。通過遺傳密碼拓展技術,在RIG-I C864位點引入非天然氨基酸,實現了分子間二硫鍵的穩定交聯。實驗結果表明,靶向穩定RIG-I二硫鍵的形成可以顯著增強宿主抗病毒免疫應答能力。同時,研究團隊通過體內外實驗證明,疾病相關的RIG-I病理突變(如C268F或E373A)或mtRNA泄漏至胞質中均能導致RIG-I異常激活,從而引發異常的固有免疫應答。RIG-I的病理突變或mtRNA引起的異常激活依賴于C864-C869位點的分子間二硫鍵形成。為此,該研究開發了靶向抑制RIG-I C864-C869分子間二硫鍵形成的干擾肽RIP-III。在相關細胞和小鼠模型中,RIP-III能夠有效抑制這些異常的RIG-I介導的免疫應答。
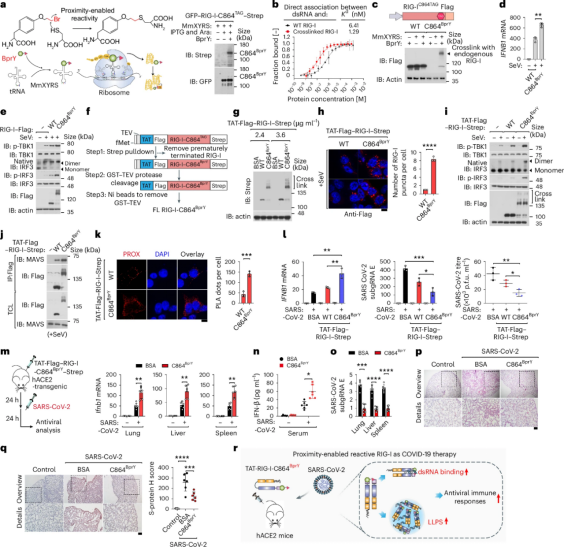
圖3. 靶向RIG-I C864-C869分子間二硫鍵以調控宿主抗病毒免疫應答
總結
該項研究首次揭示了RIG-I在響應RNA病毒感染時發生分子間二硫鍵這一過程。研究發現,RIG-I分子間C864-C869二硫鍵的形成對于其相分離及其介導的抗病毒免疫應答至關重要。此外,研究團隊開發了靶向穩定或抑制RIG-I二硫鍵形成的干預策略,為抗病毒治療及自身免疫性疾病的治療提供了新的思路。該項研究不僅為RIG-I的激活機制提供了更為深入的見解,還為開發針對RIG-I介導的相關疾病的臨床治療藥物奠定了堅實的基礎。研究中使用的賽業OriCell®提供的動物模型,為實驗的順利進行提供了重要支持。未來,基于RIG-I二硫鍵調控的抗病毒策略有望在臨床中得到廣泛應用,為人類健康保駕護航。