BCMA作為多發(fā)性骨髓瘤理想治療靶點的應(yīng)用前景及挑戰(zhàn)
引言
多發(fā)性骨髓瘤(multiple myeloma,MM)是一種惡性漿細胞疾病,在全球范圍內(nèi)每年新增病例約16萬例,發(fā)病率位居血液系統(tǒng)惡性腫瘤第二位,目前尚無根治方法。該疾病的病理特征主要表現(xiàn)為骨髓內(nèi)漿細胞單克隆性增殖并分泌異常的單克隆免疫球蛋白或其片段(M蛋白)。
盡管傳統(tǒng)治療方案如蛋白酶體抑制劑(PI)和免疫調(diào)節(jié)藥物(IMiDs)已取得顯著療效,但仍面臨患者復(fù)發(fā)率高和腫瘤細胞清除不完全等臨床挑戰(zhàn)。對于PI和IMiDs治療均無效的復(fù)發(fā)難治性多發(fā)性骨髓瘤(RRMM)患者,其中位生存期僅13個月左右,凸顯了開發(fā)新型治療策略的迫切性。研究表明,B細胞成熟抗原(BCMA)在惡性漿細胞表面特異性高表達,這一特性使其成為治療多發(fā)性骨髓瘤的理想治療靶點。
BCMA
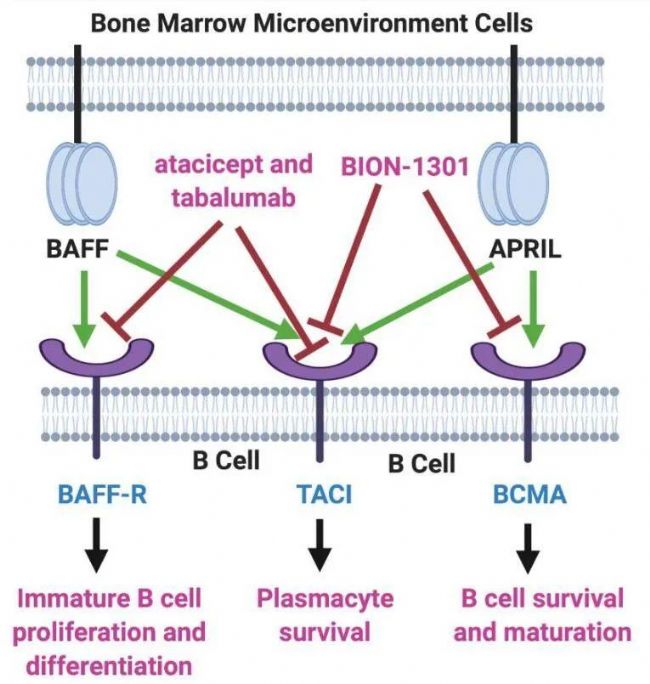
B細胞激活因子(BAFF/BLyS/TALL-1)與增殖誘導(dǎo)配體(APRIL)作為腫瘤壞死因子超家族成員,在自身免疫性疾病(如紅斑狼瘡、類風(fēng)濕關(guān)節(jié)炎)發(fā)病機制中的作用已獲廣泛認知。近年研究發(fā)現(xiàn),這兩種細胞因子在骨髓微環(huán)境中的表達對骨髓瘤細胞的存活與增殖具有關(guān)鍵調(diào)控作用。臨床觀察顯示,多發(fā)性骨髓瘤患者的疾病進展及預(yù)后與血清BAFF/APRIL水平顯著相關(guān)。從分子機制來看,BAFF和APRIL均可與骨髓瘤細胞表面的TACI及BCMA受體結(jié)合,其中BAFF還能與第三種受體BAFF-R相互作用。
BCMA(CD269/TNFRSF17)作為腫瘤壞死因子受體家族成員,其分子結(jié)構(gòu)包含三個特征性區(qū)域:通過二硫鍵穩(wěn)定的胞外區(qū)(1-54位氨基酸)、跨膜區(qū)(55-77位氨基酸)以及胞內(nèi)區(qū)(78-184位氨基酸)。在生理狀態(tài)下,BCMA的表達具有高度組織特異性,主要分布于漿細胞表面。當(dāng)漿細胞發(fā)生惡性轉(zhuǎn)化時,BCMA呈現(xiàn)顯著過表達,并通過激活NF-κB、PI3K/AKT、STAT3和MAPK等關(guān)鍵信號通路,促進腫瘤細胞生長、存活及耐藥性形成。值得注意的是,BCMA在多發(fā)性骨髓瘤各病程階段(從初治到復(fù)發(fā))均保持穩(wěn)定表達,這一特性使其成為極具開發(fā)價值的治療靶點。此外,多項研究證實BCMA不僅可作為疾病診斷和預(yù)后的生物標志物,還能預(yù)測治療反應(yīng)。
可溶性BCMA(sBCMA)是γ-分泌酶介導(dǎo)的膜蛋白剪切產(chǎn)物,在多發(fā)性骨髓瘤患者中水平升高且與不良預(yù)后相關(guān)。sBCMA包含胞外結(jié)構(gòu)域及部分跨膜區(qū),既能降低靶抗原密度,又可作為"分子誘餌"干擾抗BCMA藥物的治療效果。這一發(fā)現(xiàn)推動了γ-分泌酶抑制劑的研發(fā),該類抑制劑在阿爾茨海默病和Notch信號通路異常相關(guān)腫瘤治療中已顯現(xiàn)應(yīng)用價值,有望增強BCMA靶向治療的臨床療效。
BCMA靶點的免疫治療
當(dāng)前針對BAFF/APRIL/BCMA信號軸的治療研發(fā)主要聚焦于BCMA靶點,重點布局三大方向:單克隆抗體(包括裸抗與抗體偶聯(lián)藥物)、雙特異性抗體以及CAR-T細胞療法。
Belantamab-Mafoodin是一種ADC,其中抗體通過抗蛋白酶的馬來酰亞胺基連接物與微管抑制劑單甲基auristatin F(MMAF)偶聯(lián)。與BCMA受體結(jié)合后會干擾BAFF和APRIL信號,從而誘導(dǎo)ADCC,而細胞毒性成分能通過阻斷微管聚合抑制細胞分裂,使腫瘤細胞停止于G/M期并誘導(dǎo)caspase-3依賴的細胞凋亡。
以T細胞為基礎(chǔ)的抗體療法在對抗包括MM在內(nèi)的多種癌癥方面發(fā)揮了重要作用。兩個主要的研究領(lǐng)域在這一領(lǐng)域占據(jù)主導(dǎo)地位:T細胞結(jié)合雙特異性抗體(T-BsAb)和嵌合抗原受體(CAR)T細胞治療。伴隨T細胞活化免疫療法(包括基于T-BsAbs和CAR-T細胞形式的治療)的兩個最重要和最常遇到的不良反應(yīng)是細胞因子釋放綜合征(CRS;細胞因子風(fēng)暴)和神經(jīng)毒性(CAR-T細胞相關(guān)腦病綜合征;CRES),兩者都可能危及生命。幾乎無一例外,在免疫治療藥物的每次試驗中,都會出現(xiàn)不同嚴重程度的CRS。
嵌合抗原受體(CAR)T細胞治療在腫瘤免疫治療中占有重要地位。這種形式的過繼性細胞轉(zhuǎn)移(ACT)旨在通過重組DNA技術(shù)將患者來源的細胞毒性T細胞轉(zhuǎn)化為癌細胞的特異性殺手,通過重組DNA技術(shù)構(gòu)建病毒載體來表達針對癌細胞抗原的嵌合受體。工程化的T細胞再融合到病人體內(nèi),目的是致命地附著在靶向的惡性細胞上。盡管實體瘤仍然是一個巨大的挑戰(zhàn),但這項技術(shù)已經(jīng)成功地應(yīng)用于某些血液腫瘤,尤其是B細胞惡性腫瘤。
總結(jié)
盡管BCMA靶向治療前景廣闊,仍面臨諸多挑戰(zhàn)。包括治療耐藥機制、不良反應(yīng)管理、療效持久性等問題。未來研究將聚焦于優(yōu)化治療方案、開發(fā)新型靶向策略、探索聯(lián)合治療模式等方面。隨著科學(xué)技術(shù)的不斷進步,BCMA靶向治療有望為多發(fā)性骨髓瘤患者帶來更多治療選擇和治愈希望。
參考文獻
[1]Shah, N., Chari, A., Scott, E. et al. B-cell maturation antigen (BCMA) in multiple myeloma: rationale for targeting and current therapeutic approaches. Leukemia 2020,34: 985–1005.
[2]Cho SF, Anderson KC, Tai YT.Targeting B Cell Maturation Antigen (BCMA) in Multiple Myeloma: Potential Uses of BCMA-Based Immunotherapy[J]. Front Immunol. 2018 Aug 10;9:1821.
[3]Yu B, Jiang T, Liu D.BCMA-targeted immunotherapy for multiple myeloma [J].J Hematol Oncol. 2020 Sep 17;13(1):125.
[4]Wilcock P, Webster R.The multiple myeloma drug market[J].Nat Rev Drug Discov. 2019 Jul;18(8):579-580.
[5]GlobalData: Multiple Myeloma-Global Drug Forecast and Market Analysis to 2027.
杭州斯達特 (www.starter-bio.com)志在為全球生命科學(xué)行業(yè)提供優(yōu)質(zhì)的抗體、蛋白、試劑盒等產(chǎn)品及研發(fā)服務(wù)。依托多個開發(fā)平臺:重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發(fā)平臺(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認證、ISO9001認證、ISO13485。