去唾液酸糖蛋白受體(ASGPR)的表達(dá)機(jī)制與作用
概述
去唾液酸糖蛋白受體(ASGPR),又稱“Ashwell–Morell”受體,是最早從哺乳動(dòng)物凝集素中發(fā)現(xiàn)的一種受體。ASGPR能夠特異性高效識(shí)別以非還原半乳糖或N-乙酰半乳糖胺為末端的糖蛋白或分子。此外,ASGPR還參與細(xì)胞纖連蛋白、親血栓成分、肝脂蛋白和血清免疫球蛋白-A的攝取。ASGPR與病原體細(xì)胞成分的結(jié)合也被認(rèn)為是肝臟感染性疾病的重要原因之一。
ASGPR的表達(dá)
ASGPR主要在肝細(xì)胞中表達(dá),但在其他細(xì)胞類型中也有檢測(cè)到,包括腹腔巨噬細(xì)胞、大鼠和人類的睪丸、人類精子、腸道上皮細(xì)胞以及外周血單核細(xì)胞等。有研究表明,大腸癌的肝轉(zhuǎn)移病灶中也存在ASGPR的表達(dá)。盡管如此,肝細(xì)胞中的ASGPR表達(dá)量遠(yuǎn)高于其他組織。
ASGPR的表達(dá)可能受到多種因素的影響。例如,乙醇、四氯化碳、脂多糖和抗Fas抗體會(huì)損害肝臟中ASGPR的表達(dá)。此外,糖尿病狀態(tài)和部分肝切除也可能導(dǎo)致ASGPR功能障礙。
ASGPR與配體的結(jié)合
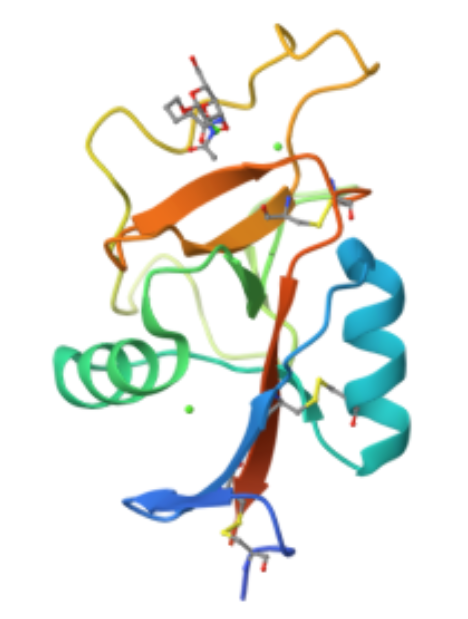
人類ASGPR由46 kDa和50 kDa兩種多肽亞基組成。每個(gè)亞基均為II型跨膜蛋白,其糖識(shí)別域(CRD)被認(rèn)為是ASGPR與非還原半乳糖殘基和N-乙酰半乳糖胺結(jié)合的關(guān)鍵區(qū)域。鈣離子在ASGPR與配體的結(jié)合中起重要作用,ASGPR的CRD含有三個(gè)鈣離子結(jié)合位點(diǎn),但其結(jié)合親和力較低。受體鈣離子與配體氧原子之間的配位鍵距離為2.8-3.0埃。
ASGPR對(duì)半乳糖(Gal)和N-乙酰半乳糖胺(GalNAc)具有高親和力。其H1型亞基的活性結(jié)合位點(diǎn)包括天冬氨酸241、天冬氨酸265、天冬酰胺264、谷氨酸252、谷氨酰胺239和色氨酸243等氨基酸殘基。這些位點(diǎn)通過酰胺鍵和羧基側(cè)鏈與半乳糖的3位和4位羥基形成氫鍵。天然配體(如阿拉伯半乳聚糖和普魯蘭多糖)由于含有多個(gè)糖二聚體,能夠形成更多的氫鍵,從而增強(qiáng)與ASGPR的結(jié)合。此外,ASGPR亞基的三維結(jié)構(gòu)預(yù)測(cè)顯示,寡聚糖可能通過三觸角結(jié)合模式與受體結(jié)合。
ASGPR的內(nèi)化
ASGPR通過與配體結(jié)合,在肝細(xì)胞質(zhì)膜表面形成網(wǎng)格蛋白包被的囊泡,并通過網(wǎng)格蛋白介導(dǎo)的內(nèi)吞作用內(nèi)化。Gal/GalNAc與ASGPR的結(jié)合依賴于pH 6的環(huán)境和鈣離子的存在。配體與ASGPR結(jié)合后,觸發(fā)網(wǎng)格蛋白包被的小窩形成,隨后ASGPR迅速內(nèi)化,其內(nèi)化速率常數(shù)為3.4×10⁸,半衰期約為3分鐘。
內(nèi)化過程中,Dynamin蛋白通過水解GTP驅(qū)動(dòng)網(wǎng)格蛋白包被的囊泡(直徑約100-120 nm)從質(zhì)膜上脫離。囊泡脫去網(wǎng)格蛋白包被后,ASGPR可被重復(fù)利用。多個(gè)內(nèi)體融合形成管狀腔室和囊泡,其pH值約為6。隨后,這些內(nèi)體被分選至回收內(nèi)體或早期溶酶體小泡中。溶酶體酶從高爾基體轉(zhuǎn)運(yùn)至成熟溶酶體,其pH值降至5.4,削弱了鈣離子與ASGPR的結(jié)合力,導(dǎo)致配體從ASGPR-配體復(fù)合物中釋放。去唾液酸糖蛋白配體在溶酶體中被降解,而ASGPR則免受破壞。
內(nèi)吞過程受多種理化常數(shù)的影響,如解離常數(shù)和配體密度等。循環(huán)內(nèi)體能夠保護(hù)質(zhì)膜表面的ASGPR,使其半衰期在質(zhì)膜上可達(dá)約20小時(shí)。
產(chǎn)品信息
杭州斯達(dá)特 (www.starter-bio.com)志在為全球生命科學(xué)行業(yè)提供優(yōu)質(zhì)的抗體、蛋白、試劑盒等產(chǎn)品及研發(fā)服務(wù)。依托多個(gè)開發(fā)平臺(tái):重組兔單抗、重組鼠單抗、快速鼠單抗、重組蛋白開發(fā)平臺(tái)(E.coli,CHO,HEK293,InsectCells),已正式通過歐盟98/79/EC認(rèn)證、ISO9001認(rèn)證、ISO13485。
- CD47-SIRPα/CD172a作為免疫檢查點(diǎn)的作用機(jī)制及其腫瘤治療潛力
- 生物素標(biāo)記蛋白的方法及應(yīng)用
- Biacore分子互作分析系統(tǒng)的原理及應(yīng)用
- 重組人β-細(xì)胞素在肝癌侵襲轉(zhuǎn)移研究中的應(yīng)用及案例分享
- BCMA作為多發(fā)性骨髓瘤理想治療靶點(diǎn)的應(yīng)用前景及挑戰(zhàn)
- ASGR1作為高膽固醇血癥治療新靶點(diǎn)的作用機(jī)制、研究突破與未來趨勢(shì)
- 肝臟去唾液酸糖蛋白受體(ASGPR)的結(jié)構(gòu)、功能及臨床應(yīng)用
- 去唾液酸糖蛋白受體(ASGPR)的表達(dá)機(jī)制與作用
- MCE中國抗體實(shí)驗(yàn)圖征稿啟示,秀美圖贏AirPods
- 斯達(dá)特生物將亮相2025年美國AACR展會(huì),誠邀您蒞臨!
- MCE直播預(yù)告:銅死亡的機(jī)制探索與醫(yī)學(xué)應(yīng)用
- 2024第九屆疫苗中國領(lǐng)導(dǎo)者年會(huì)通知
- MCE推出超900種一抗和多種二抗產(chǎn)品,涵蓋熱門靶點(diǎn)
- 丹納赫將收購Abcam以推動(dòng)生命科學(xué)領(lǐng)域研究創(chuàng)新進(jìn)程
- 睿捷生物新學(xué)期新福利,四重優(yōu)惠限時(shí)享
- 佰諾全景科研mIHC病理技術(shù)服務(wù)年中大促銷火熱來襲